Ecuación Química.
Reactivo 1 + Reactivo 2 -----------------> Producto
Sustancias que interactúan entre sí en una reacción química; se escriben en el lado izquierdo de la ecuación química. Antes de la punta de la flecha.
(Daud/Carrillo/Montagut, 2005)
Productos:
Sustancias que se forman durante una reacción química; se escriben en el lado derecho de la ecuación química. Después de la punta de la flecha.
(Daud/Carrillo/Montagut, 2005)
Catalizador:
Sustancia que modifica la velocidad (acelera) de una reacción química y que al término de ésta se recupera sin cambio.
(Daud/Carrillo/Montagut, 2005)
Sólo la acelera, propicia o retiene, NO interviene en la Reacción Química.
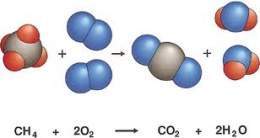
Simbología de las ecuaciones químicas.
¿Cómo leer una ecuación química?
Reacción química.
Una reacción químicas es el proceso químico es que dos sustancias, denominados reactivos, por la acción de un factor energético, se convierte en otras sustancias designadas como productos.
(definicionabc, sf)
Tipos de Reacciones químicas.
Adición o síntesis:
Consiste es que dos o más reactantes forman un solo producto. En este tipo de reacciones generalmente se libera calor, es decir, son exotérmicas.
(Full quimica, 2011)
Ej.
H₂O + SO₃ ----------→ H₂SO₄
En este tipo de reacción química un determinado compuesto se descompone es sustancias más simples o en los elementos que lo constituyen.
(escolares, sf)
Ej.
2HgO -----------→ 2Hg + O₂
Sustitución simple:
Se presenta cuando un elemento químico más activo o menos activo desplaza a otro menos reactivo que se encuentra formando parte del compuesto.
(Prezi, 2015)
Ej.
Na + H₂O -------------→ NaOH + H₂
Doble sustitución:
Son aquellas en que dos elementos que se encuentran en compuestos diferentes intercambian sus posiciones dos nuevos compuestos según la fórmula:
AB + CD ------------→ CB + AD
(quimicas.net, 2015)
Ej.
HBr + Ca(OH)₂ ---------------→ CaBr + H₂O
Combustión:
Reacción entre un comburente y un combustible, con desprendimiento de luz y calor.
(Medeiros, 2007)
Lluvia ácida y sus reacciones químicas.
Se producen diversos gases y algunos son los óxidos de nitrógeno y el dióxido de azufre, que reaccionan al contacto con la humedad del aire y se transforman en ácido sulfúrico (H2SO4), ácido nítrico (HNO3) y ácido clorhídrico (HCl). Estos ácidos se depositan en las nubes y se produce la lluvia ácida.
El dióxido de carbono, naturalmente en la atmósfera es ácido, pero se vuelve mucho más ácido debido a los ácidos que se arrojan a la atmósfera. Su pH es entre 5 y 6, pero este cambia a 3 e incluso a 2 debido a los ácidos.
La oxidación adicional de los óxidos de azufre y de nitrógeno puede ser catalizada por los contaminantes atmosféricos, incluyendo las partículas sólidas y por la luz solar. Una vez formados los óxidos SO3 y NO2, reaccionan con facilidad con la humedad atmosférica para formar el ácido sulfúrico y nítrico respectivamente. Le imparten características ácidas a la atmósfera y estas se precipitan con la neblina, la lluvia o la nieve.
(Reacciones ácido-base, s.f.)
Balanceo de Ecuaciones.
El balanceo de las ecuaciones químicas, consiste en establecer la cantidad de sustancias que intervienen en una reacción química para que correspondan con la cantidad de sustancias producidas, es decir, que los elementos que reaccionan en el primer miembro de la ecuación son los mismos que quedan después de la reacción en el segundo miembro de la ecuación.
(Ejemplode.com, 2016)
Método de Tanteo.
En este método se intenta equilibrar el número de átomos en la ecuación química, modificando los valores de las sustancias presente de uno o ambos lados, para que exista igualdad entre el número de átomos de los reactivos y los productos. Es un método de ensayo y error.
Se debe tomar en cuenta que todo lo que entra en una reacción debe salir, así como lo que sale debe de haber entrado, si ésto no pasa, dicha reacción NO existe.
(Ejemplode.com, 2016)
Pasos:
1. Se toman en cuenta los radicales de los reactivos, así como de los productos. Veamos las siguiente reacción de neutralización del sulfato de sodio con el ácido clorhídrico:
Na2SO3 + HCl -- > NaCl + H2O + SO2
2. Comenzaremos por identificar el número de átomos de cada elemento en ambos lados de la ecuación:
Reactivos: Na = 2; S = 1; O = 3; H = 1; Cl = 1
Productos: Na = 1; S = 1; O = 3; H = 2; Cl = 1
3. Para balancear una ecuación al tanteo, tenemos que seguir las siguientes reglas:
a. No agregaremos elementos que no pertenezcan a la ecuación.
b. No modificaremos los radicales de los elementos de la ecuación, es decir, si de un lado el hidrógeno tiene un radical 2, debe seguir con el radical 2.
c. Sí podemos expresar al aumento de átomos agregando el número de átomos de alguno de los compuestos de la mezcla. Así, si queremos expresar que hay 4 átomos de ácido clorhídrico, escribiremos 4HCl.
d. Es conveniente comenzar el balanceo por los elementos que sólo aparecen una vez en cada miembro, dejando al último los que aparecen más de una vez, si es necesario.
e. El hidrógeno y el oxígeno son de los últimos elementos a considerar para el balanceo.
4. No tenemos un lugar definido para comenzar nuestro balanceo, así que podemos comenzar por cualquiera de los miembros de la ecuación. Comenzaremos con los átomos de sodio. Como vemos, en los reactivos hay dos átomos de sodio para reaccionar en la molécula de sulfato de sodio, mientras que del lado de los productos, en el cloruro de sodio, sólo hay un átomo de sodio. Esto significa que para equilibrar el sodio y que haya dos átomos en el resultado, debe haber dos moléculas de cloruro de sodio en el lado de los productos. Así tendríamos:
2 + 1 + 3 + 1+ 1 -- > 2 +2 + 2 + 1 + 1 + 2
Na2SO3 + HCl -- > 2NaCl + H2O + SO2
5.Como vemos, ya tenemos la misma cantidad de átomos de sodio. Pero nuestra ecuación sigue desequilibrada. En efecto, ahora tenemos:
Reactivos: Na = 2; S = 1; O = 3; H = 1; Cl = 1
Productos: Na = 2; S = 1; O = 3; H = 2; Cl = 2
6. Ahora tenemos dos átomos de cloro en el producto y sólo uno en los reactivos. Si consideramos que el resultado de la reacción produce dos átomos de sal, y sólo hay un átomo de cloro en los reactivos, significa que ahora debemos considerar que actúan dos moléculas del compuesto que contiene el cloro, o sea, dos moléculas de ácido clorhídrico. Para comprobar si nuestra suposición es cierta, agregamos a nuestra fórmula la indicación de que están reaccionando dos átomos de HCl y volvemos a contar los átomos:
2 + 1 + 3 + 2 + 2 -- > 2 +2 + 2 + 1 + 1 + 2
Na2SO3 + 2HCl -- > 2NaCl + H2O + SO2
7.Ahora ya tenemos el mismo número de átomos reaccionando de uno y otro lado de la ecuación. Finalmente revisamos que en ambos lados exista el mismo número de átomos de cada elemento:
Reactivos: Na = 2; S = 1; O = 3; H = 2; Cl = 2
Productos: Na = 2; S = 1; O = 3; H = 2; Cl = 2
Tenemos el mismo número de átomos de cada elemento en ambos lados de la ecuación, lo que significa que nuestra fórmula está correctamente balanceada.
(Ejemplode.com, 2016)












Método algebraico.
Este método es un proceso matemático que consiste en asignar literales a cada una de las sustancias, crear ecuaciones en función de los átomos y al resolver las ecuaciones, determinar el valor de los coeficientes.
(González, 2010)
Pasos:
1. Se les asigna una letra a cada uno de los compuestos.
NaOH + H2SO4 -----------> Na2SO4 + H2O
a b c d
2. Se cuantifica y determina cuantos átomos hay de cada elemento sustituyendo el nombre del mismo por la letra asignada. Si un elemento se repite en los reactivos, éstos se suman, si hay en ambos lados; reactivos y productos, éstos se igualan.
Na O H S
a = 2c a + 4b = 4c + d a + 2b = 2d b = c
3. Verificar qué letra se repite más y asignarle cualquier valor (de preferencia que sea 1), si se repiten 2 o más letras el mismo número de veces, se escoge por orden alfabético. Se sustituyen los valores y se resuelven estas ecuaciones. En caso de quedar una fracción se multiplica TODO hasta que se tengan números enteros.
a = 1 b = c a + 2b = 2d a = 1 * 2 = 2
a = 2c b = 1/2 1 + 2(1/2) = 2d b = 1/2 * 2 = 1
1 = 2c 1 + 1 = 2d c = 1/2 * 2 = 1
c = 1/2 d = 1 d = 1 * 2 = 2
4. Los números dados de los valores de las letras se ponen en su lugar correspondiente de la ecuación química.
2NaOH + H2SO4 ------------> Na2SO4 + 2H2O
Al momento de cuantificar de nuevo, tenemos el mismo número de átomos en los reactivos y productos.
(Figueroa, 2016)
Método Oxidación-Reducción (REDOX).
La oxidación es un evento que se presenta en un átomo cuando éste pierde o cede electrones, provocando que su número de oxidación (valencia) aumente en su carácter positivo.
La reducción es un evento simultáneo a la oxidación, ya que ante la pérdida de electrones por un átomo es necesario que otro átomo gane esos electrones, provocando la reducción; al ganar electrones un átomo hace que su número de oxidación (valencia) disminuya, o bien, se haga más negativo.
La oxidación es un evento que se presenta en un átomo cuando éste pierde o cede electrones, provocando que su número de oxidación (valencia) aumente en su carácter positivo.
La reducción es un evento simultáneo a la oxidación, ya que ante la pérdida de electrones por un átomo es necesario que otro átomo gane esos electrones, provocando la reducción; al ganar electrones un átomo hace que su número de oxidación (valencia) disminuya, o bien, se haga más negativo.
**La pérdida de electrones es la oxidación, la ganancia de electrones es la reducción.**
Método REDOX.
- El número de oxidación de un elemento libre es cero (Zn°, Al°, Cu°, N2°, O2°, Cl2°, P4°, H2°).
- El número de oxidación de los metales en los compuestos es igual a su valencia iónica. Por ejemplo: los metales alcalinos tienen un número de oxidación de +1, los metales alcalinotérreos de +2, y siempre es positiva, algunos metales tienen valencia única como los que pertenecen a los grupis IA (1), IIA (2) y IIA (3), pero otros tienen valencias variables y los encontramos en el bloque de los metales de transición.
- El número de oxidación de un ión es igual a su carga.
- El número de oxidación del Hidrógeno en la mayoría de los compuestos es de +1, excepto en los hidruros metálicos, que son compuestos en donde el hidrógeno se une al metal y es en este caso donde el hidrógeno es -1.
- El número de oxidación del oxígeno en la mayoría de los compuestos que forma es -2, excepto H2O, en donde es -1.
- La suma algebraica de los números de oxidación de todos los átomos en un compuesto es igual a cero.
- Para este tipo de balanceo, es conveniente auxiliarnos de:

- Sólo se deben modificar dos elementos cuando se tienen las valencias de los átomos es decir; sólo puede haber dos valencias diferentes de dos átomos.
- Siempre que una ecuación lleva agua está desbalanceada, para esto después de REDOX se utiliza tanteo.
- El átomo que se redujo osea ganó electrones es el agente oxidante y el que se oxidó es decir perdió electrones es el agente reductor.
- El número de electrones ya sea perdidos o ganados debe de ser igual para poder balancear la ecuación.
- Dónde están puestos los átomos que cambian de valencia son denominados semirreacciones.
Velocidad de Reacción.
Tres condiciones requeridas para que ocurra una reacción.
- Colisión: Los reactivos deben chocar.
- Orientación: Los reactivos deben alinearse de manera adecuada para romper y formar enlaces.
- Energía: La colisión debe proporcionar la energía de activación.
Velocidad de reacción.
La velocidad (o rapidez) de reacción se determina al medir la cantidad de un reactivo agotado, o la cantidad de un producto formado, en un determinado tiempo.
Factores que afectan la velocidad de Reacción.
Naturaleza de los Reactivos.
Estado de agregación:
El choque de las moléculas se ve favorecido si las moléculas reaccionantes están en el mismo estado físico. Los medios líquidos o gaseosos favorecen las colisiones. Si uno de los reactivos es sólido es necesario disminuir el tamaño de las partículas.
El choque de las moléculas se ve favorecido si las moléculas reaccionantes están en el mismo estado físico. Los medios líquidos o gaseosos favorecen las colisiones. Si uno de los reactivos es sólido es necesario disminuir el tamaño de las partículas.
(Slideshare.net, 2015)
Concentración.
Si los reactivos están en disolución o son gases encerrados en un recipiente, cuanto mayor sea su concentración, más alta será la velocidad de la reacción en la que participen, ya que, al haber más partículas en el mismo espacio, aumentará el número de colisiones.
El ataque que los ácidos realizan sobre algunos metales con desprendimiento de hidrógeno es un buen ejemplo, ya que este ataque es mucho más violento cuanto mayor es la concentración del ácido.
(Sánchez, 2015)
Temperatura.
Al aumentar la temperatura, también lo hace la velocidad a la que se mueven las partículas, y por tanto, aumentará el número de colisiones y la violencia de éstas. El resultado es una mayor velocidad de reacción. Se dice, de manera aproximada, que por cada 10°C de aumento en la temperatura, la velocidad se duplica.
(Sánchez, 2015)
Presión.
"A temperatura constante, un aumento de presión favorece la contracción de volumen".
El aumento de la presión sobre un sistema en equilibrio se traslade, o sea, el equilibrio traslade para el lado de menor volumen y la disminución de presión hace que el equilibrio se traslade en el lado de mayor volumen.
Cuanto menor sea la presión ejercida sobre un líquido es más fácil la vaporización.
Si aumenta la presión, la colisión aumenta.
(González, 2010)
Tamaño de la partícula.
Si el tamaño de las partículas son pequeñas, entonces la superficie de ellos aumenta. El aumento de superficie de los reactivos aumenta la velocidad de reacción.
(serife, s.f.)

Catalizadores.
Son sustancias que aumentan o disminuyen la rapidez de una reacción sin transformarse. La forma de acción de los mismos es modificando el mecanismo de reacción, empleando pasos elementales con mayor o menor energía de activación. En ningún caso el catalizador provoca la reacción química; no varía su calor de reacción. Los catalizadores se añaden en pequeñas cantidades y son muy específicos; es decir, cada catalizador sirve para determinadas reacciones. El catalizador se puede recuperar al final de la reacción, puesto que no es reactivo ni participa en la reacción.
(Sánchez, 2015)
**La velocidad de una reacción aumenta si:
- Se aumenta la temperatura
- La concentración de una disolución reactivo se incrementa
- La presión de un gas de reacción se incrementa
- Los reactivos sólidos se fragmentan en pedazos más pequeños
- Se utiliza un catalizador
Bibliografía
definicionabc. (sf de sf de sf). definicionabc.com. Recuperado el 1 de septiembre de 2016, de definicionabc.com: http://www.definicionabc.com
escolares. (sf de sf de sf). escolares. Recuperado el 13 de agosto de 2016, de escolares: www.escolares.net
Full quimica. (sf de noviembre de 2011). Fullquimica. Recuperado el 13 de agosto de 2016, de fullquimica: www.fullquimica.com
fullquimica. (s.f.). fullquimica.com.
Medeiros, L. (13 de septiembre de 2007). quimymas. Recuperado el 5 de septiembre de 2016, de quimymas: www.quimymas.blogspot
Prezi. (5 de MAYO de 2015). Prezi. Recuperado el 13 de agosto de 2016, de Prezi: https://prezi.com
quimicas.net. (sf de mayo de 2015). quimicas. Recuperado el 13 de agosto de 2016, de quimicas: www.quimicas.net
angelicacienciaatualcancez.blogspot.com
aprendiendoquimica2enmss.blogspot.com
http://es.slideshare.net
ejemplode.com, (2016), "Ejemplo de Balanceo de ecuaciones por tanteo", recuperado el 26 agosto, 2016 de: www.ejemplode.com
González, I. (2010), Balanceo de ecuaciones químicas, recuperado el 29 agosto 2016 de: es.slideshare.net
Reacciones ácido-base (s.f.), La lluvia ácida y sus reacciones, recuperado el 30 de agosto, 2016 de: reaccionesacidos-bases.spaces.com
Reosso, V. (2009), Cinética Química, recuperado el 06 de septiembre, 2016 de: es.slideshare.net
Sánchez, J. 82015), Factores que afectan a la velocidad de reacción, recuperado el 30 agosto 2016 de: elfisicoloco.blogspot.mx
González, M (2010), Efecto de la presión-Ley de Boyle- Mariotte, recuperado el 30 agosto 2016, de: química.laguia2000.com
Serife, E. (s.f.), Factores que afectan la velocidad de reacción, recuperado el 30 agosto, 2016 de: www.chemistrytutorials.org
Trabajo elaborado por:
Ximena López Ruiz.
Yaritza Figueroa Aguilar.
Adela Andrea Martínez Torres.
Nahomi Ortiz Rentería.
Profesora:
Hilda Lucía Cisneros López.
Escuela de Nivel Medio Superior de Salvatierra.